


Qu’est-ce que le COVID long ?
Le COVID long, également appelé séquelles post-aiguës du COVID-19 (PASC), est un terme utilisé pour décrire les symptômes et les complications multisystémiques que certaines personnes ressentent après une infection grave par le SRAS-CoV-2. Alors que la plupart des gens se remettent du COVID-19 en quelques semaines, d’autres continuent de ressentir des symptômes pendant des mois, voire plus. On estime qu’environ 10 % des personnes infectées souffrent d’une COVID longue, ce qui représente au moins 65 millions d’individus dans le monde, l’incidence étant plus élevée chez les personnes hospitalisées (environ 50 à 70 % des cas). Les causes exactes du long COVID ne sont pas encore entièrement comprises, et il n’existe actuellement aucun remède ni traitement pour cette maladie. Ici, nous explorons la physiopathologie du long COVID et les modèles animaux précliniques qui peuvent être utilisés pour mieux comprendre cette maladie et tester les traitements candidats.
Symptômes et causes sous-jacentes du COVID long
Le COVID long peut affecter plusieurs systèmes organiques, notamment les systèmes respiratoire, cardiovasculaire, neurologique et gastro-intestinal. Certains des symptômes les plus courants du COVID long comprennent la fatigue, l’essoufflement, les douleurs thoraciques, les palpitations, les douleurs abdominales, les nausées, les troubles cognitifs, la perte de mémoire, les acouphènes et le dysfonctionnement du système reproducteur.
Les causes de ces symptômes font encore l’objet d’investigations et sont soupçonnées d’être multiples et potentiellement superposées. Il a été suggéré que les contributeurs à la pathogenèse pourraient inclure :
- maintien des réservoirs à long terme du SRAS-CoV-2 dans les tissus tels que les poumons, le cœur ou le cerveau ;
- dérégulation du système immunitaire, y compris auto-immunité ; impact sur le microbiote ;
- dérégulation de la coagulation; et la neuroinflammation.
Une infection persistante peut entraîner une inflammation chronique et des lésions tissulaires, entraînant des symptômes à long terme.
Il est important de noter que la grande majorité des patients atteints de COVID long n’ont pas été hospitalisés pour leur infection initiale par le SRAS-CoV-2, ce qui entraîne des difficultés spécifiques pour le suivi à long terme de ces patients « COVID-19 légers ». Il existe de nombreux défis liés aux problématiques de diagnostic et de dépistage du COVID long, comme un certain manque de connaissance des séquelles non respiratoires du COVID-19 parmi les professionnels de santé, et des lacunes dans l’identification et le suivi de ce groupe spécifique de patients.
Modèles précliniques de COVID long
Compte tenu de la compréhension partielle actuelle de cette maladie complexe, une exploration expérimentale de la physiopathologie du COVID long est nécessaire. Mieux imiter les symptômes dans les modèles de laboratoire est crucial pour le développement préclinique d’interventions thérapeutiques efficaces.
Peu de temps après le début de la pandémie de SARS-CoV-2, et sur la base des travaux antérieurs effectués au moment de l’épidémie de SARS-CoV, des efforts majeurs ont été lancés pour donner accès à une variété de modèles animaux de laboratoire, y compris des souris (génétiquement modifiées). modèles, hamsters syriens dorés, furets et primates non humains. Aucun de ces modèles ne récapitule complètement tous les aspects de la maladie humaine, car chaque espèce a tendance à développer de manière reproductible une certaine gravité des symptômes. En d’autres termes, l’hétérogénéité des symptômes et de la gravité de la maladie observée chez l’homme ne peut pas être observée dans un modèle animal donné. Pourtant, ces modèles animaux montrent généralement la présence virale dans les tissus situés en dehors des voies respiratoires, par exemple dans le cœur, le tractus gastro-intestinal, les reins et le système nerveux central. En outre, des lésions à long terme des poumons et d’autres tissus, en particulier du cœur, des reins et du cerveau, ont été signalées, par exemple chez les hamsters. De tels dommages pourraient être la conséquence d’une réplication virale locale ou de réponses immunitaires locales excessives. Sur la base de ce profil de maladie à long terme et multiorganique, de tels modèles expérimentaux sont attrayants pour l’étude des COVID long . Néanmoins, chacune des espèces disponibles peut récapituler de manière plus appropriée uniquement certains aspects du COVID long (Figure 1).
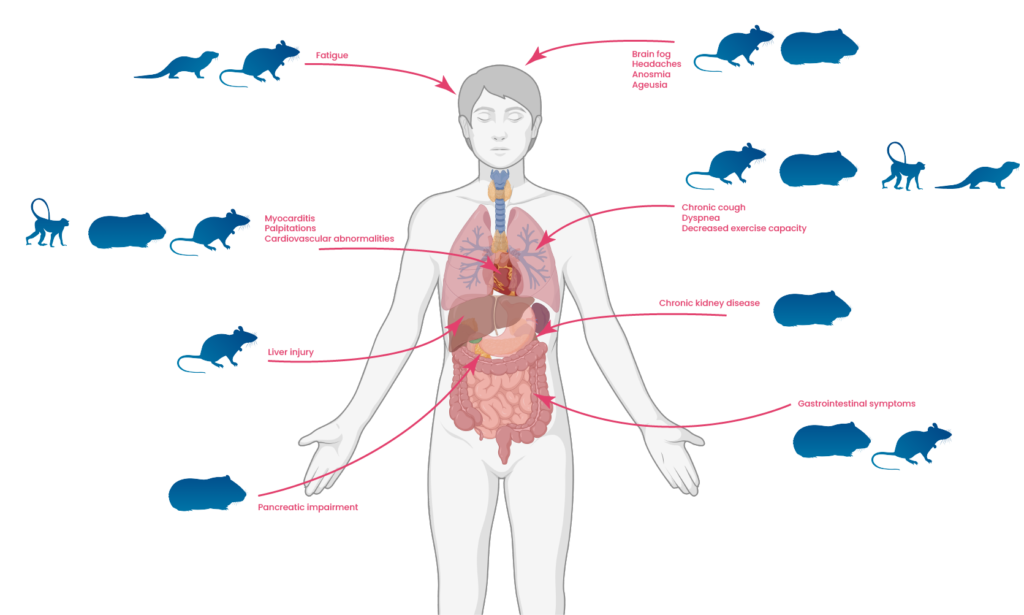
Figure 1. Animals models for specific aspects of long COVID.
Conclusion
Le COVID long est une maladie multisystémique complexe encore mal comprise, ayant un impact significatif sur la qualité de vie des individus touchés. Décrypter la physiopathologie du COVID long est crucial pour développer des traitements efficaces contre cette maladie. Les modèles précliniques sont des outils essentiels pour comprendre les mécanismes sous-jacents au COVID long et tester les traitements potentiels, et une sélection minutieuse du modèle optimal est nécessaire en fonction de la question de recherche.
A propos de l’auteur
Cet article a été rédigé par Nicolas Legrand, PhD. Dans son rôle actuel chez Oncodesign Services, Nicolas est chef du département de pharmacologie translationnelle et est impliqué dans les programmes de R&D sur les maladies inflammatoires, auto-immunes et infectieuses.
-
References
Davis HE et al. Long COVID: major findings, mechanisms and recommendations. Nat Rev Microbiol. (2023), 21:133.
https://pubmed.ncbi.nlm.nih.gov/36639608/
Frere JJ et al. SARS-CoV-2 infection in hamsters and humans results in lasting and unique systemic perturbations after recovery. Sci Transl Med. (2022), 14:eabq3059.
https://pubmed.ncbi.nlm.nih.gov/35857629/
Jansen EB et al. After the virus has cleared – Can preclinical models be employed for long COVID research? PLoS Pathog. (2022), 18:e1010741.
https://pubmed.ncbi.nlm.nih.gov/36070309/
Käufer C et al. Microgliosis and neuronal proteinopathy in brain persist beyond viral clearance in SARS-CoV-2 hamster model. EBioMedicine (2022), 79:103999.
https://pubmed.ncbi.nlm.nih.gov/35439679/
Munoz-Fontela C. et al. Animals models for COVID-19. Nature (2020), 586:509.
https://pubmed.ncbi.nlm.nih.gov/32967005/
Part of Figure 1 was created with BioRender.com
