

La pharmaco-imagerie, des études non-invasives à l’appui de la preuve de concept en pharmacologie
En pharmacologie, l’imagerie est un outil non-invasif qui permet de réduire considérablement le nombre d’animaux testés et de contrôler efficacement :
- La biodistribution des médicaments
- L’expression et l’engagement de cibles in vivo
- L’effet de traitements thérapeutiques
- Leur mécanisme d’action
- Leur pharmacodynamique
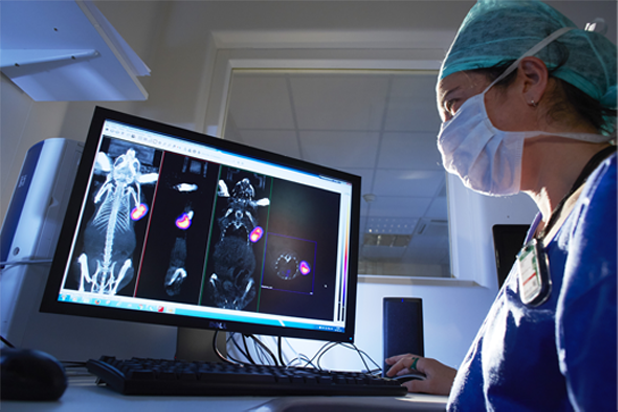

Oncodesign Services a intégré l’imagerie à sa plateforme de pharmacologie dès 2004, ajoutant au fil des ans des capacités multimodales :
- IRM 4,7 T
- Imagerie nucléaire (TEP-TDM, TEMP-TDM, TEP-IRM)
- Imagerie optique (Bioluminescence, Fluorescence)
- Échographie
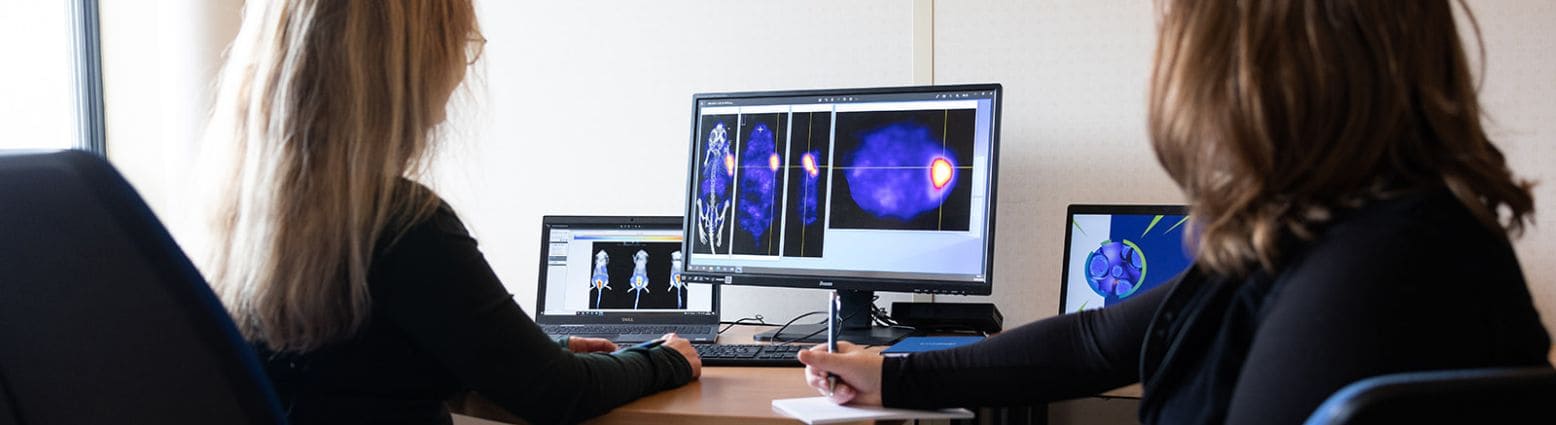
La plateforme d’imagerie multimodale in vivo d’Oncodesign Services peut être utilisée pour réaliser des études de biodistribution, détecter des tumeurs et suivre l’activité de biomarqueurs. Les études de pharmaco-imagerie emploient fréquemment des radioisotopes et s’appuient sur nos capacités en termes de bioconjugaison et radiochimie. Ces capacités peuvent être mises à profit sur des molécules, des biologiques et des nanoparticules.
DRIVE-MRT: une solution premium de « médecine nucléaire » en oncologie
DRIVE-MRT fait partie de notre amélioration continue du soutien intégré à la découverte de médicaments. Oncodesign Services et ses partenaires stratégiques Covalab, CheMatech et ABX-CRO mettent leur expertise au service de la rationalisation, de la conception et de l’optimisation d’agents radiopharmaceutiques ciblés.

Pharmimage® – des fonctionnalités de pharmaco-imagerie non-invasives
Le module technologique Pharmimage® d’Oncodesign Services est un module de pharmaco-imagerie, conçu pour suivre l’effet des traitements et définir des biomarqueurs translationnels d’efficacité en médecine de précision. Il permet de répondre aux questions qui se posent à l’aide de techniques corps entier non-invasives :
- La cible est-elle exprimée ? (Diagnostic de la pathologie, hétérogénéité de l’expression de la cible, distribution de la cible dans un cancer métastatique, CNS, cardiologie…)
- Le médicament atteint-il la cible ? (Pharmacocinétique, biodistribution, passage de la barrière hémato-encéphalique, …)
- La cible est-elle inhibée/activée, induisant des changements biochimiques et biologiques ?
(Pharmacodynamique, immunomonitoring, dose biologique optimale, …) - Existe-t-il des toxicités et des interactions médicamenteuses potentielles ?
(Sécurité, étude sur les associations médicamenteuses, métabolisme, …) - Ces changements sont-ils liés à un critère clinique ? (Efficacité d’un nouveau traitement, suivi de la réponse immunitaire à un vaccin, apparition du phénomène de résistance en médecine de précision, …)
- Peut-on déterminer des sous-populations de patients répondeurs ? (Biomarqueur translationnel)